Две вакцины от Эболы прошли проверку на безопасность
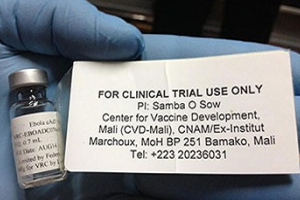 Две экспериментальные вакцины от вируса Эбола успешно прошли первый этап фазы II/III клинических испытаний в Либерии с участием более 600 человек.
Две экспериментальные вакцины от вируса Эбола успешно прошли первый этап фазы II/III клинических испытаний в Либерии с участием более 600 человек.
Клинические исследования спонсирует Национальный институт аллергии и инфекционных заболеваний США (NIAID).
Клинические испытания фазы II/III начались в либерийской столице Монровии 2 февраля 2015 года. На безопасность и эффективность испытывались две вакцины – cAd3-EBOZ и VSV-ZEBOV. Первая – совместная разработка Национального института аллергии и инфекционных заболеваний США (NIAID) и компании GlaxoSmithKline. Вторая создана Государственным агентством здравоохранения Канады, а права на нее принадлежат американской компании Merck.
Волонтеры были случайным образом поделены на три группы: первые получили одну инъекцию вакцины cAd3-EBOZ, другие – VSV-ZEBOV, а третьи – плацебо. В исследовании использовался двойной слепой метод, то есть ни испытуемые, ни делавшие инъекции медработники не знали, что вводится – вакцина или плацебо.
Для продолжения испытаний число волонтеров увеличат до полутора тысяч волонтеров. В некоторой степени это вызвано желанием увеличить число женщин, участвующих в исследовании. Сейчас их только 16%.
Ранее планировалось для этих целей набрать 27 тысяч волонтеров, но из-за снижения количества случаев заболевания руководители исследований приняли решение, что с научной точки зрения будет правильнее расширить границы клинических испытаний и вовлечь в исследование другие страны Западной Африки. Пока окончательное решение обсуждается.
Эпидемия лихорадки Эбола начала распространяться в странах Западной Африки чуть больше года назад – в феврале 2014-го.
Источник: Vademecum
Фото с сайта: independent.co.uk